Los medicamentos homeopáticos son preparados farmacéuticos obtenido por técnicas homeopáticas, conforme a las reglas descritas en las farmacopeas oficiales aceptadas en el país, con el objeto de prevenir, aliviar, curar, tratar y/o rehabilitar una condición médica.
Los fitoterapéuticos son productos medicinales empacados y etiquetados, cuyas sustancias activas provienen de plantas medicinales o asociaciones de estas o de extractos, tinturas o aceites, presentado en estado bruto o en forma farmacéutica que se utiliza con fines terapéuticos. En su formulación, no pueden contener principios activos aislados y químicamente definidos.
Los suplementos dietarios son productos cuyo propósito es adicionar a la dieta normal y ser fuente concentrada de nutrientes y otras sustancias con efecto fisiológico o nutricional.
La composición de este tipo de productos puede estar dada por vitaminas, minerales, proteínas, aminoácidos, otros nutrientes y derivados de nutrientes, plantas, concentrados y extractos de plantas solas o en combinación.
La evaluación farmacéutica tiene por objeto conceptuar sobre la capacidad técnica del fabricante del proceso de fabricación y de la calidad del producto.
La evaluación legal comprende el estudio jurídico de la documentación que se allega por parte del interesado para la concesión del registro y su conformidad con las normas legales que regulan dichas materias.
Los medicamentos homeopáticos son los preparados farmacéuticos obtenidos por técnicas homeopáticas (dinamizaciones), conforme a las reglas descritas en las farmacopeas oficiales aceptadas en el país, con el objeto de prevenir la enfermedad, aliviar, curar, tratar y/o rehabilitar un paciente. Los envases, rótulos, etiquetas y empaques hacen parte integral del medicamento, por cuanto estos garantizan su calidad, estabilidad y uso adecuado.
Con el fin de facultar a una persona natural o jurídica para producir, comercializar, importar, exportar, envasar, procesar y/o expender medicamentos homeopáticos elaborados en cantidades industriales en un laboratorio farmacéutico, es necesario obtener el registro sanitario otorgado por el Invima.
- Decreto 1229 de 2015 - Por el cual se modifica el artículo 9 del Decreto número 1737 de 2005 modificado por el Decreto número 1861 de 2006.
- Decreto 4664 de 2006 - Por el cual se modifica el Decreto 1737 de 2005 y se dictan otras disposiciones. (Elaboración y dispensación de Medicamentos Homeopáticos magistrales y Oficinales en consultorios).
- Decreto 1861 de 2006 - Por el cual se modifica y adiciona el Decreto 3554 de 2004 y se dictan otras disposiciones.
- Decreto 1737 de 2005 - Por el cual se reglamenta la preparación, distribución, dispensación, comercialización, etiquetado, rotulado y empaque de los medicamentos homeopáticos magistrales y oficinales y se dictan otras disposiciones.
- Decreto 162 de 2004 - Por el cual se modifica el artículo 3 del Decreto 549 de 2001.
- Decreto 3554 de 2004 - Por el cual se regula el régimen de registro sanitario, vigilancia y control sanitario de los medicamentos homeopáticos para uso humano y se dictan otras disposiciones.
- Decreto 549 de 2001 - Por el cual se establece el procedimiento para la obtención del certificado de cumplimiento de la Buenas Prácticas de Manufactura por parte de los laboratorios fabricantes de medicamentos que se importen o produzcan en el país.
- Decreto 334 de 2022 - Por el cual se establecen disposiciones para la renovación, modificación y suspensión de registros sanitarios de medicamentos de lintesis química, gases medicinales, biológicos y homeopáticos.
- Decreto 335 de 2022 - Por el cual se establece el procedimiento para la obtención de los certificados de cumplimiento de las buenas prácticas de elaboración, laboratorio y manufactura ante el Instituto Nacional de Vigilancia de Medicamentos y Alimentos - INVIMA.
- Resolución 3665 de 2009 - Por la cual se adopta la guía de verificación de cumplimiento de Buenas Prácticas de Manufactura de Medicamentos Homeopáticos y se dictan otras disposiciones.
- Resolución 4594 de 2007 - Por la cual se expide el Manual de Buenas Prácticas de Manufactura para Medicamentos Homeopáticos y se dictan otras disposiciones.
- Formato de registro de notificación electrónica (AIC-NOT-FM002)
- Formulario único para presentación de solicitudes de registros sanitarios de productos fitoterapéuticos, medicamentos homeopáticos y suplementos dietarios – ass-rsa-fm001 – versión 06
- ASS-RSA-GU73 guía para presentar modificaciones administrativo-legales de medicamentos de síntesis química, radiofármacos, gases medicinales, biológicos y homeopáticos (decreto 334 de 2022 modificado por el decreto 1474 de 2023)
- ASS-RSA-GU80-GUÍA PARA LA PRESENTACIÓN DE MODIFICACIONES DE SEGURIDAD Y EFICACIA AL REGISTRO SANITARIO PARA MEDICAMENTOS HOMEOPÁTICOS DE LA DIRECCIÓN DE MEDICAMENTOS Y PRODUCTOS BIOLÓGICOS
- ASS-RSA-GU81-GUÍA DE PRESENTACIÓN DE SOLICITUDES DE MODIFICACIONES DE CALIDAD AL REGISTRO SANITARIO DE MEDICAMENTOS HOMEOPÁTICOS
¿Qué es un medicamento homeopático?
De acuerdo a la normatividad vigente en materia de medicamentos homeopáticos, Decreto 3554 de 2004 y Decreto 1861 de 2006, es el preparado farmacéutico obtenido por técnicas homeopáticas, conforme a las reglas descritas en las farmacopeas oficiales aceptadas en el país, con el objeto de prevenir la enfermedad, aliviar, curar, tratar y/o rehabilitar un paciente. Los envases, rótulos, etiquetas y empaques hacen parte integral del medicamento, por cuanto estos garantizan su calidad, estabilidad y uso adecuado.
¿Cómo se clasifican los medicamentos homeopáticos?
Para efecto de la expedición del registro sanitario los medicamentos homeopáticos se clasifican en:
- Medicamentos homeopáticos simples.
- Medicamentos homeopáticos complejos.
¿Qué son los medicamentos homeopáticos simples?
Es el medicamento homeopático preparado a partir de una sola cepa homeopática o tintura madre, conforme a una de las farmacopeas oficiales en Colombia que lo contenga.
¿Qué son los medicamentos homeopáticos complejos?
Es aquel medicamento homeopático conformado por:
- La mezcla de dos o más dinamizaciones de una misma cepa homeopática, tintura madre o triturado.
- La mezcla de dos o más dinamizaciones de diferentes cepas homeopáticas, tinturas madre o triturados.
¿Todos los medicamentos homeopáticos requieren de Registro Sanitario para su comercialización?
Los medicamentos homeopáticos, elaborados en laboratorios farmacéuticos debidamente certificados en Buenas Prácticas de Manufactura de Medicamentos Homeopáticos, requieren para su producción, importación, exportación, envase, empaque, expendio, distribución y comercialización, registro sanitario expedido por el Instituto Nacional de Vigilancia de Medicamentos y Alimentos (Invima), previo el cumplimiento de los requisitos establecidos en los Decreto 3554 de 2004 y 1861 de 2006.
¿Cuál es la vigencia de un registro sanitario?
La vigencia de un registro sanitario es por diez (10) años.
¿El registro sanitario de un medicamento homeopático, es susceptible de ser renovado?
Si. Las renovaciones de los registros sanitarios de los medicamentos homeopáticos se realizarán siguiendo el mismo procedimiento descrito para su otorgamiento. La solicitud deberá radicarse ante el Invima como mínimo con tres (3) meses de anterioridad al vencimiento del registro.
Toda solicitud de renovación de un registro sanitario que no sea presentada en el término aquí previsto, se tramitará como nueva solicitud de registro sanitario.
¿Cuáles son las modalidades de registro sanitario de medicamentos homeopáticos?
El registro sanitario se podrá expedir para las siguientes modalidades:
- Fabricar y vender
- Importar y vender
- Importar, acondicionar y vender
- Fabricar y exportar
La modalidad de fabricar y vender comprende por sí misma la posibilidad de exportar sin perjuicio de que la autoridad sanitaria competente pueda expedir el correspondiente registro sanitario exclusivamente para la modalidad de fabricar y exportar.
El Invima, a petición del interesado, podrá otorgar a un mismo producto, registro sanitario, para las modalidades de fabricar y vender o importar y vender, cuando la composición del producto importado sea idéntica a la del producto de fabricación local y no implique alteraciones del medicamento homeopático. La información técnica debe sustentar la modalidad respectiva, incluidos los estudios de estabilidad.
Los medicamentos homeopáticos cuyo registro sanitario se solicite bajo la modalidad de importar, acondicionar y vender deberán cumplir con los requisitos señalados para la modalidad de importar y vender. El registro sanitario bajo la modalidad de importar, acondicionar y vender se otorgará para aquellos medicamentos homeopáticos que se importen y que a nivel local realicen una de las siguientes operaciones:
- Envase y empaque del producto a granel
- Empaque del producto previamente envasado
¿Cómo se puede identificar un registro sanitario de un medicamento homeopático en el mercado?
Para efectos de garantizar la vigilancia y control de los medicamentos homeopáticos, la codificación de los registros será para los medicamentos homeopáticos simples MHS-antepuesto del año de expedición y para los medicamentos homeopáticos complejos MHC-antepuesto del año de expedición.
Los medicamentos homeopáticos a los cuales se les otorgue registro sanitario en la modalidad de fabricar y exportar no podrán en ningún caso ser comercializados en Colombia, la codificación de los registros sanitarios expedidos bajo la modalidad de fabricar y exportar será RSMH Exp. Cuando estos medicamentos quieran ser comercializados en Colombia deberán obtener registro sanitario para fabricar y vender.
¿Qué documentación se requiere para obtención de un registro sanitario de medicamentos homeopáticos simples del régimen simplificado?
El registro sanitario simplificado ampara a las diferentes diluciones preparadas a partir de la misma cepa homeopática y bajo la misma forma farmacéutica.
Para efectos de la obtención del registro sanitario simplificado, el interesado deberá presentar el formato de solicitud de registro sanitario ante el Instituto Nacional de Vigilancia de Medicamentos y Alimentos (Invima) adjuntando la documentación establecida en el Artículo 18 del Decreto 1861 de 2006.
¿Qué condiciones deben reunir los medicamentos homeopáticos simples del régimen simplificado?
Los medicamentos homeopáticos simples de fabricación nacional e importada, preparados a partir de la misma cepa homeopática en sus diferentes diluciones y con la misma forma farmacéutica, se ampararán bajo un sólo registro sanitario simplificado siempre y cuando cumplan con las siguientes condiciones:
- Que su vía de administración sea oral o externa.
- Ausencia de indicación terapéutica particular en la etiqueta o en cualquier información relativa al medicamento.
- El preparado no deberá contener más de una parte por 1.000 de tintura ni más de la centésima parte de la dosis más baja que eventualmente se emplee en medicina alopática, de aquellas sustancias activas cuya presencia en un medicamento alopático o fitoterapéutico implique la obligatoriedad de presentar fórmula médica.
- Que la cepa o tintura madre se encuentren en una de las farmacopeas homeopáticas oficialmente aceptadas en el presente Decreto.
¿Qué requisitos se necesitan para la obtención de un registro sanitario de medicamentos homeopáticos complejos?
Para la expedición del registro sanitario de los medicamentos homeopáticos complejos y simples de régimen no simplificado se deberá cumplir con los siguientes requisitos:
- Evaluación farmacéutica, que tiene por objeto conceptuar sobre la idoneidad técnica del fabricante, del proceso de fabricación y de la calidad del producto.
- Evaluación legal, que consiste en el estudio jurídico de la documentación que se allega por parte del interesado para la concesión del registro sanitario y su conformidad con las normas legales que regulan dichas materias.
- Evaluación de la utilidad terapéutica, que comprende el procedimiento por el cual la autoridad sanitaria se forma un juicio sobre la utilidad, conveniencia y seguridad de un medicamento homeopático.
¿Qué documentación se requiere para obtención de un registro sanitario de medicamentos homeopáticos simples de régimen no simplificado y complejos nacionales?
Para efectos de la obtención del registro sanitario simplificado, el interesado deberá presentar el formato de solicitud de registro sanitario ante el Inivma, adjuntando la documentación establecida en los artículos 26, 27 y 29 del Decreto 3554 de 2004.
¿Qué documentación se requiere para obtención de un registro sanitario de medicamentos homeopáticos simples de Régimen no simplificado y complejos importados?
El interesado deberá radicar la solicitud de registro sanitario, a la cual deberá anexar para efectos de la evaluación farmacéutica, la documentación técnica, avalada por el director técnico o responsable técnico del establecimiento fabricante, contenida en el artículo 26 del presente Decreto 3554 de 2004, con excepción de la presentación de los registros de producción. Para efecto de la evaluación legal, se deberán anexar los documentos señalados en los literales a), b), c), e), g) y h) del artículo 27 del Decreto 3554 de 2004. Además de lo indicado anteriormente, se deberá anexar lo señalado en el literal i) del artículo 27 y para efectos de la evaluación de la utilidad terapéutica, la documentación prevista en el artículo 29 del presente Decreto 3554 de 2004.
Tener presente los criterios de Evaluación de la Utilidad Terapéutica, señalados en el Artículo 24 del Decreto 1861 de 2006:
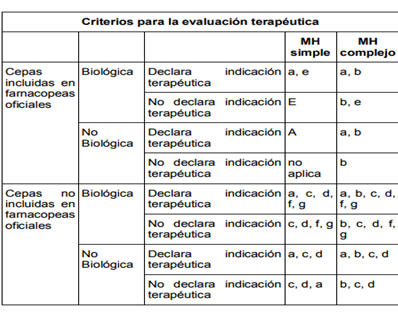
- Los estudios clínicos y toxicológicos que sustenten la indicación propuesta, la seguridad y eficacia del preparado.
- La justificación y sustentación de la combinación de las diferentes cepas en sus respectivas diluciones apoyada en documentación científica.
- La monografía de la(s) cepa(s) no farmacopeicas conforme a lo establecido en el artículo 21 del presente Decreto 1861 de 2006.
- El informe del uso homeopático de la cepa, basado en estudios de experimentación patogenésico o documento correspondiente a alguna de las entidades sanitaria u organizaciones avaladas por las mismas, de los países de referencia que certifiquen el uso homeopático de dicha cepa.
- Los requisitos establecidos en el artículo 39 del Decreto 3554 de 2004.
- El certificado emitido por la autoridad sanitaria competente así como el fabricante del producto donde conste que la cepa(s) fue sometida(s) a todos los controles que permitan demostrar o asegurar que no existe ningún riesgo de transmisión de enfermedades por la utilización de cepas de origen humano, animal o microorganismo.
- El requisito establecido para los productos biológicos de los artículos 21 y 22 del presente decreto.
Entiéndase por documentación científica, las materias médicas homeopáticas, monografías de los componentes aceptados por las autoridades sanitarias competentes de los países de referencia de que trata el presente decreto y publicaciones de carácter científica reconocida.
¿Los medicamentos homeopáticos que son preparados magistrales, cuentan con una regulación específica?
Los medicamentos homeopáticos magistrales se encuentran amparados por la Normatividad vigente colombiana, Decreto 1737 del 2005, “Por el cual se reglamenta la preparación, distribución, dispensación, comercialización, etiquetado, rotulado y empaque de los medicamentos homeopáticos magistrales y oficinales y se dictan otras disposiciones”.
¿Qué condiciones deben reunir los medicamentos homeopáticos simples del régimen simplificado?
Sin perjuicio de las condiciones exigidas en el decreto para la obtención de registro sanitario de los medicamentos homeopáticos simples y complejos de fabricación nacional o importada, se deberá cumplir además con las condiciones que a continuación se describen:
Indicar vía de administración
Ausencia de indicación terapéutica particular en la etiqueta, en cualquier información o literatura relativa al medicamento; en caso, tal que sea de venta con fórmula médica.
Que su grado de dilución garantice la inocuidad del medicamento; en particular, la preparación no deberá contener más de una parte por 1000 de tintura madre, salvo lo establecido en una de las farmacopeas homeopáticas oficialmente aceptadas.
¿Bajo cual normatividad se pueden regir los medicamentos homeopáticos que son preparados magistrales?
Los medicamentos homeopáticos magistrales se rigen bajo el Decreto 1737 del 2005, “Por el cual se reglamenta la preparación, distribución, dispensación, comercialización, etiquetado, rotulado y empaque de los medicamentos homeopáticos magistrales y oficinales y se dictan otras disposiciones”.
¿Las preparaciones magistrales de medicamentos homeopáticos requieren de áreas especiales para su elaboración en Colombia?
Los medicamentos homeopáticos magistrales no se realizan en laboratorios por lo cual no requieren de áreas especiales. Sin embargo, es de tener en cuenta que son elaborados en las farmacias homeopáticas de nivel II que son aquellas farmacias homeopáticas legalmente autorizadas que además de las actividades desarrolladas por las farmacias de Nivel I, disponen de la infraestructura y capacidad técnica, operativa y de calidad para la preparación de medicamentos homeopáticos magistrales y oficinales en formas farmacéuticas no estériles. Estas farmacias podrán surtir únicamente a nivel nacional las necesidades de los medicamentos homeopáticos magistrales y oficinales requeridas por las farmacias homeopáticas de Nivel I y II y otros puntos de venta autorizados para medicamentos oficinales como farmacias-droguerías, servicios farmacéuticos y droguerías legalmente autorizadas. La dirección técnica de estas farmacias estará a cargo de un químico farmacéutico.
¿Un laboratorio certificado con Buenas Prácticas de Elaboración para fórmulas magistrales puede asegurar la calidad técnica, normativa y regulatoria para elaborar fórmulas magistrales de medicamentos homeopáticos?
Los medicamentos homeopáticos magistrales no se elaboran en laboratorios. Estos son elaborados en las farmacias homeopáticas de nivel II legalmente autorizadas que además de las actividades desarrolladas por las farmacias de nivel I, disponen de la infraestructura y capacidad técnica, operativa y de calidad para la preparación de medicamentos homeopáticos magistrales y oficinales en formas farmacéuticas no estériles.
Estas Farmacias podrán surtir únicamente a nivel nacional las necesidades de los medicamentos homeopáticos magistrales y oficinales requeridas por las farmacias homeopáticas de nivel I y II y otros puntos de venta autorizados para medicamentos oficinales como farmacias-droguerías, servicios farmacéuticos y droguerías legalmente autorizadas. La dirección técnica de estas farmacias estará a cargo de un químico farmacéutico.
¿Se requiere autorización por parte de Invima para proceder con la elaboración de medicamentos homeopáticos magistrales en las mismas áreas donde elaboran medicamentos magistrales estériles?
Los medicamentos homeopáticos magistrales no podrán ser estériles, por tanto no existen áreas para dicha elaboración en esa forma farmacéutica.
Productos fitoterapéuticos
Con el fin de facultar a una persona natural o jurídica para producir, comercializar, importar, exportar, envasar, procesar y/o expender este tipo de productos, es necesario que obtenga ante el Invima el registro sanitario en cualquiera de sus categorías tanto para preparaciones farmacéuticas con base en plantas medicinales (PFM) como para productos fitoterapéuticos tradicionales (PFT), conforme el procedimiento tendiente a verificar el cumplimiento de los requisitos técnico-legales establecidos en la normatividad sanitaria vigente disponible en este sitio, al igual que los formatos de solicitud, el listado de plantas medicinales con fines terapéuticos y establecimientos con certificación de cumplimiento de las Buenas Prácticas de Manufactura autorizados para su fabricación y acondicionamiento.
- Resolución 662 de 2011 - Por la cual se modifica la Resolución 126 de 2009, modificada por la Resolución 527 de 2010 y se dictan otras disposiciones. (Tiendas naturistas)
- Resolución 527 de 2010 - Por la cual se modifica el parágrafo del artículo 6° y el artículo 13 de la Resolución 126 de 2009. (Tiendas naturistas)- Por la cual se establecen las condiciones esenciales para la apertura, funcionamiento, vigilancia y control sanitario de las tiendas naturistas y se dictan otras disposiciones.
- Resolución 2834 de 2008 - Por la cual se adopta el Vademécum de Plantas Medicinales Colombiano y se establecen los lineamientos para su actualización.
- Resolución 5107 de 2005 - Por la cual se adopta el instrumento de verificación de cumplimiento de condiciones sanitarias para los laboratorios que elaboren productos Fito terapéuticos.
- Resolución 3131 de 1998 - Por la cual se adopta el Manual de Buenas Prácticas de Manufactura de productos farmacéuticos con base en recursos naturales vigentes.
- Decreto 2266 de 2004 - Por el cual se reglamentan los regímenes de registros sanitarios, y de vigilancia y control sanitario y publicidad de los productos fitoterapéuticos.
- Decreto 3553 de 2004 - Por el cual se modifica el Decreto 2266 de 2004 y se dictan otras disposiciones.
- Decreto 162 de 2004 - Por el cual se modifica el artículo 3 del Decreto 549 de 2001.
- Decreto 2510 de 2003 - Por el cual se modifica el artículo 13 del Decreto 677 de 1995 y se dictan otras disposiciones.
- Decreto 549 de 2001 - Por la cual se establecen las condiciones esenciales para la apertura, funcionamiento, vigilancia y Por el cual se establece el procedimiento para la obtención del certificado de cumplimiento de la Buenas Prácticas de Manufactura por parte de los laboratorios fabricantes de medicamentos que se importen o produzcan en el país.
- Decreto 335 de 2022 - Por el cual se establece el procedimiento para la obtención de los certificados de cumplimiento de las buenas prácticas de elaboración, laboratorio y manufactura ante el Instituto Nacional de Vigilancia de Medicamentos y Alimentos - INVIMA.
- Decreto 1156 de 2018 - Por el cual se reglamenta el régimen de registro sanitario de productos Fitoterapéuticos y se dictan otras disposiciones.
Año 2019
- Metodología en la realización del listado de plantas
- Metodología en la realización del listado de plantas publicación No. 1
- Respuesta a observaciones listado de plantas
- Respuesta a observaciones listado de plantas publicación No. 1
- Listado de plantas medicinales aceptadas con fines terapéuticos
Año 2019
- Listado de Plantas Medicinales Aceptadas con Fines Terapéuticos 16-06-2019
- Listado de Plantas Medicinales Aceptadas con Fines Terapéuticos 31-12-2018
- Listado de Plantas Medicinales Aceptadas con Fines Terapéuticos 31-07-2018
Año 2017
- Listado de Plantas Medicinales Aceptadas con Fines Terapéuticos 28-12-2017
- Listado de Plantas Medicinales Aceptadas con Fines Terapéuticos 17-08-2017
Año 2016
- Listado de Plantas Medicinales Aceptadas con Fines Terapéuticos 21-12-2016
- Listado de Plantas Medicinales Aceptadas con Fines Terapéuticos 20-09-2016
¿Qué es un producto fitoterapéutico?
De acuerdo a la normatividad vigente, Decreto 2266 de 2004 y Decreto 3553 de 2004, un producto fitoterapéutico es el producto medicinal empacado y etiquetado, cuyas sustancias activas provienen de material de la planta medicinal o asociaciones de estas, presentado en estado bruto o en forma farmacéutica que se utiliza con fines terapéuticos. También puede provenir de extractos, tinturas o aceites.
No podrá contener en su formulación principios activos aislados y químicamente definidos. Los productos obtenidos de material de la planta medicinal que haya sido procesado y obtenido en forma pura no serán clasificados como productos fitoterapéutico.
¿Cómo se clasifican los productos fitoterapéuticos?
Los productos fitoterapéuticos para efectos de registro sanitario se clasifican en:
- Preparaciones farmacéuticas con base en plantas medicinales.
- Producto fitoterapéutico tradicional.
- Producto fitoterapéutico de uso tradicional importado
¿Qué son las Preparaciones farmacéuticas con base en plantas medicinales?
Es el producto fitoterapéutico elaborado a partir de material de la planta medicinal, o preparados de la misma, a la cual se le ha comprobado actividad terapéutica y seguridad farmacológica y que está incluido en las normas farmacológicas colombianas vigentes. Su administración se realiza para indicaciones o uso terapéutico definido y se utiliza para la prevención, alivio, diagnóstico, tratamiento, curación o rehabilitación de la enfermedad.
¿Qué es un producto fitoterapéutico tradicional?
Es aquel producto fitoterapéutico de fabricación nacional elaborado a partir de material de planta medicinal o asociaciones entre sí, cultivadas en nuestro país en las formas farmacéuticas aceptadas cuya eficacia y seguridad, aun sin haber realizado estudios clínicos, se deduce de la experiencia por su uso registrado a lo largo del tiempo y en razón de su inocuidad está destinado para el alivio de manifestaciones sintomáticas de una enfermedad.
¿Qué es un producto fitoterapéutico tradicional importado?
Es aquel producto fitoterapéutico que no es de fabricación nacional, elaborado a partir de planta medicinal o asociaciones entre sí, en las formas farmacéuticas aceptadas, cuya eficacia y seguridad, aun sin haber realizado estudios clínicos, se deduce de la experiencia por su uso registrado a lo largo del tiempo y que en razón de su inocuidad, está destinado para el alivio de manifestaciones sintomáticas de una enfermedad.
¿Qué requieren los productos fitoterapéuticos para su comercialización?
Los productos fitoterapéuticos, requieren para su fabricación, producción, importación, exportación, procesamiento, envase, empaque, expendio y comercialización de registro sanitario expedido por el Invima. Este registro sanitario se expedirá por producto.
¿Cuál es la vigencia de un registro sanitario?
La vigencia de un registro sanitario es por diez (10) años.
¿El registro sanitario de un producto fitoterapéutico, es susceptible de ser renovado?
Si. Las renovaciones de los registros sanitarios se realizarán siguiendo el mismo procedimiento de su expedición, para lo cual requerirá de la documentación técnica y legal de acuerdo a su categoría. La solicitud de renovación deberá radicarse ante el Invima al menos con tres (3) meses de anterioridad al vencimiento del registro sanitario.
Toda solicitud de renovación de un registro sanitario que no sea presentada en el término aquí previsto, se tramitará como nueva solicitud de registro sanitario.
¿Cuáles son las modalidades de registro sanitario?
Las modalidades de registro sanitario son:
- Fabricar y vender
- Importar y vender
- Importar, acondicionar y vender
- Fabricar y exportar
- La modalidad de fabricar y vender comprende por sí misma la posibilidad de exportar.
La modalidad importar y vender al igual que importar, acondicionar y vender no aplica por su naturaleza a los productos fitoterapéuticos tradicionales. Estas modalidades, se aplicarán a los demás productos fitoterapéuticos.
¿Cómo se puede identificar un registro sanitario de productos fitoterapéuticos en el mercado?
Para efectos de garantizar la vigilancia y control de los productos fitoterapéuticos, la codificación de los registros será para las preparaciones Farmacéuticas con base en plantas medicinales: PFM antepuesto al año de expedición, para productos fitoterapéuticos tradicional: PFT antepuesto al año de expedición y para los productos fitoterapéuticos de uso tradicional importados, PFTI- antepuesto al año de expedición.
¿Cómo es el trámite de un registro sanitario de un producto fitoterapéutico clasificado como preparación farmacéutica con base en plantas medicinales?
En primer lugar, el interesado debe tener presente que el producto cumpla con las siguientes condiciones:
- Ser aprobado por la Sala Especializada de Productos Naturales o quien haga sus veces o estar incluidos en el listado de plantas medicinales aceptadas con fines terapéuticos de uso medicinal;
- No presentarse en formas farmacéuticas inyectables u oftálmicas y en general aquellas formas farmacéuticas en las que se requiera esterilidad;
- No contener en su formulación sustancias con actividad estupefaciente o psicotrópica;
- No combinarse el material de la planta medicinal con sustancias activas aisladas y químicamente definidas.
Para efectos de registro sanitario, el interesado debe presentar la solicitud de registro sanitario ante el Invima con la documentación legal y farmacéutica establecida en los 25 y 26 del Decreto 2266 de 2004, según la modalidad (fabricar y vender, importar y vender o importar, acondicionar y vender). Si el material de la planta medicinal utilizada en la preparación farmacéutica con base en plantas medicinales no se encuentra incluida en el listado de plantas medicinales aceptadas con fines terapéuticos o no ha sido aceptado por la Comisión Revisora, se deberá radicar primero la solicitud de evaluación para inclusión en el listado de plantas medicinales aceptadas con fines terapéuticos ante la Sala Especializada de Productos Naturales o quien haga sus veces en los términos y condiciones enunciados en los Artículos 27 a 29 del mencionado Decreto. Con el concepto favorable de la Sala Especializada, el solicitante deberá radicar la documentación farmacéutica y legal mencionada anteriormente.
Los formatos de solicitud para diligenciar pueden ser consultados en la siguiente ruta en el sitio web del Invima / Trámites y servicios / Trámites /Seleccione el tipo de producto (producto fitoterapéutico) / seleccionar trámite (registro sanitario) / formatos
¿Cómo es el trámite de un registro sanitario de un producto fitoterapéutico clasificado como producto fitoterapéutico tradicional?
En primer lugar, el interesado debe tener presente que el producto cumpla con las siguientes condiciones:
- Presentarse en tisanas o en las formas farmacéuticas aceptadas exceptuando las formas farmacéuticas estériles (inyectables y oftálmicas).
- Las plantas medicinales utilizadas para la elaboración de estos productos deberán estar incluidas en el vademécum colombiano de plantas medicinales. En el evento de no encontrarse en el vademécum colombiano de plantas medicinales será la Sala Especializada de Productos Naturales o quien haga sus veces la encargada de aprobarlas e incluirlas.
- Su alegación de uso no se relaciona con la identificación de uno o más principios activos, sino con la definición cualitativa de ingredientes y marcadores.
- No contendrá en su formulación sustancias con actividad estupefaciente o psicotrópica.
- No combinará el material de la planta medicinal con sustancias activas aisladas y químicamente definidas.
- Los componentes activos provenientes de material de la planta medicinal que ha sido procesado y obtenido en forma pura, no será clasificado como producto fitoterapéutico tradicional.
Para efectos de registro sanitario, el interesado debe presentar la solicitud de registro sanitario ante el Invima con la documentación legal y farmacéutica establecida en los artículos 34 y 35 del Decreto 2266 de 2004. Si el material de la planta medicinal utilizada o el producto fitoterapéutico tradicional no se encuentra incluido en el vademécum de plantas medicinales colombianas o no ha sido aceptado por la Sala Especializada de Productos Naturales de la Comisión Revisora, se debe radicar primero la solicitud de evaluación para aprobación e inclusión en el vademécum colombiano de Plantas Medicinales ante la Sala Especializada de Productos Naturales de la Comisión Revisora en los términos y condiciones enunciados en los artículos 32 y 33 del mencionado decreto. Posteriormente, una vez cuente con el concepto favorable de la Sala Especializada, se debe radicar la documentación farmacéutica y legal mencionada anteriormente.
Con el fin de facultar a una persona natural o jurídica para producir, comercializar, importar, exportar, envasar, procesar y/o expender suplementos dietarios, es necesario obtener el registro sanitario ante el Invima conforme al procedimiento tendiente a verificar el cumplimiento de los requisitos técnico-legales establecidos en la normatividad sanitaria vigente disponible en este sitio al igual que los formatos de solicitud, listado de declaraciones de propiedades aceptadas para suplementos dietarios y establecimientos autorizados para su fabricación, entre otros documentos técnicos.
- Resolución 2015 de 2011 - Por la cual se expide la Guía de Inspección de Buenas Prácticas de Manufactura en plantas o fábricas de alimentos que fabriquen, acondicionen o semielaboren suplementos dietarios y se dictan otras disposiciones.
- Resolución 3096 de 2007 - Por la cual se establece el reglamento técnico sobre las condiciones y requisitos que deben cumplir los suplementos dietarios que declaren o no información nutricional, propiedades nutricionales, propiedades de salud o cuando su descripción produzca el mismo efecto de las declaraciones de propiedades nutricionales o de las declaraciones de propiedades en salud.
- Decreto 272 de 2009 - Por el cual se modifica el parágrafo del artículo 24 del Decreto 3249 de 2006, modificado por el artículo 6o del Decreto 3863 de 2008.
- Decreto 3249 de 2006 - Por el cual se reglamenta la fabricación, comercialización, envase, rotulado o etiquetado, régimen de registro sanitario, de control de calidad, de vigilancia sanitaria y control sanitario de los suplementos dietarios, se dictan otras disposiciones y se deroga el Decreto 3636 de 2005.
- Decreto 335 de 2022 - Por el cual se establece el procedimiento para la obtención de los certificados de cumplimiento de las buenas prácticas de elaboración, laboratorio y manufactura ante el Instituto Nacional de Vigilancia de Medicamentos y Alimentos - INVIMA
- Decreto 3863 de 2008 - Por el cual se modifica el Decreto 3249 de 2006 y se dictan otras disposiciones.
- Decreto 549 de 2001 - Por el cual se establece el procedimiento para la obtención del Certificado de Cumplimiento de la Buenas Prácticas de Manufactura por parte de los laboratorios fabricantes de medicamentos que se importen o produzcan en el país.
CODEX ALIMENTARUIS
- NORMAS OFICIALES DEL CODEX ALIMENTARIUS: http://www.fao.org/fao-who-codexalimentarius/codex-texts/list-standards/en/
- CÓDIGO DE ADITIVOS ALIMENTARIOS: http://www.fao.org/gsfaonline/additives/index.html?lang=en
EUFUS
- EAFUS - A FOOD ADDITIVE DATABASE. LISTADO GRAS: https://www.cfsanappsexternal.fda.gov/scripts/fdcc/?set=FoodSubstances
FOOD ADDITIVE STATUS LIST
- FOOD ADDITIVE STATUS LlST: https://www.fda.gov/food/food-additives-petitions/food-additive-status-list
BOTINICAL GRAS
FOOD AND DRUGS
- PART 172 - FOOD ADDITIVES PERMITTED FOR DIRECT ADDITION TO FOOD FOR HUMAN CONSUMPTION. Subpart D - Special Dietary and Nutritional Additives:
https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfcfr/CFRSearch.cfm?CFRPart=172 - PART 182 - SUBSTANCES GENERALLY RECOGNIZED AS SAFE: https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfcfr/CFRSearch.cfm?CFRPart=182
- ENZYME PREPARATIONS USED IN FOOD (PARTIAL LIST):
https://www.fda.gov/food/generally-recognized-safe-gras/enzyme-preparations-used-food-partial-list - PART 184 - DIRECT FOOD SUBSTANCES AFFIRMED AS GENERALLY RECOGNIZED AS SAFE: https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfcfr/CFRSearch.cfm?CFRPart=184
FDA - SEA FOOD LIST:
- FDA - SEA FOOD LIST: https://www.accessdata.fda.gov/scripts/fdcc/?set=seafoodlist
- ACEITES ESENCIALES, OLEORRESINAS (LIBRES DE SOLVENTES) Y EXTRACTOS NATURALES (INCLUYENDO DESTILADOS):
https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfcfr/CFRSearch.cfm?fr=182.20 - LISTADO GRAS: GRAS Substances (SCOGS) Database: https://www.accessdata.fda.gov/scripts/fdcc/?set=SCOGS
DIRECTIVAS DE LA COMISION EUROPEA
- DIRECTIVAS GENERALES DE LA COMISIÓN EUROPEA: https://ec.europa.eu/food/safety/labelling_nutrition/supplements_en
- Commission Directive 2001/15/EC: http://eur-lex.europa.eu/legal-content/EN/TXT/?qid=1510155667658&uri=CELEX:32001L0015
- Commission Directive 2004/5/EC: http://eur-lex.europa.eu/legal-content/EN/TXT/?qid=1510155450665&uri=CELEX:32004L0005
- Commission Directive 2004/6/EC: http://eur-lex.europa.eu/legal-content/EN/TXT/?qid=1510155332618&uri=CELEX:32004L0006
- Commission Directive 2006/34/EC: http://eur-lex.europa.eu/legal-content/EN/TXT/?qid=1510155255662&uri=CELEX:32006L0034
- Commission Directive 2002/46/EC: http://eur-lex.europa.eu/legal-content/EN/TXT/?uri=CELEX:32002L0046
LEGISLACIÓN COLOMBIANA
Listado de Plantas Tóxicas
Listado de nuevos Ingredientes
- ¿Qué son los suplementos dietarios?
- Son aquellos productos cuyo propósito es adicionar a la dieta normal y que son fuente concentrada de nutrientes y otras sustancias con efecto fisiológico o nutricional que puede contener vitaminas, minerales, proteínas, aminoácidos, otros nutrientes y derivados de nutrientes, plantas, concentrados y extractos de plantas solas o en combinación.
- Es importante saber que los suplementos dietarios al momento de su aprobación y comercialización no deben estar brindando una información que no sea veraz respecto a la naturaleza del producto, presentándose los productos empleando palabras, ilustraciones u otras representaciones gráficas que puedan dar lugar a apreciaciones falsas sobre la naturaleza, origen, composición o calidad del producto, de acuerdo con Decreto 3249 de 2006 ni declarar propiedades que no puedan comprobarse, o que señalen que los productos son útiles para prevenir, aliviar, tratar o curar una enfermedad, trastorno o estado fisiológico.
- ¿Dónde puedo encontrar información para importar un suplemento dietario y tramitar el registro en Colombia?
- En la sección de tramites podrá encontrar información relevante en cuanto a los requisitos generales, técnicos y legales referente al diligenciamiento que debe realizar el usuario acorde a su necesidad de elaborar, comercializar, importar, exportar, envasar, procesar, y vender los productos que lo requieren de acuerdo con la normatividad sanitaria vigente. También podrá encontrar información asociada sobre las normas que los regula, formatos requeridos, tarifas que aplican y el sitio donde puede radicar la información.
- ¿Cuáles son los requisitos para la fabricación y comercialización de los suplementos dietarios?
- Los requisitos para la fabricación y comercialización de los suplementos dietarios están contemplados en el Artículo 1 del Decreto 3863 de 2008.
- ¿Dónde puedo encontrar información sobre el rotulado de los productos suplementos dietarios?
- Los requisitos sobre el rotulado de los productos suplementos dietarios están contemplados en el Artículo 4 del Decreto 3863 de 2008.
Debe además tener en cuenta que para la obtención del registro sanitario de los suplementos dietarios nacionales o importados, de conformidad con el numeral 2.2 del Artículo 11 del Decreto 3249 de 2006, el interesado deberá adjuntar los artes definitivos de etiquetas, que incluyan las leyendas obligatorias, que deberán ajustarse a las disposiciones contenidas en el título VI (Art. 19 y ss.) del Decreto 3249 de 2006, en concordancia con los Artículos 4, 5 y11 del Decreto 3863 de 2008 y Artículo 1 del Decreto 272 de 2009. Además, para la aprobación del Registro Sanitario, el producto necesariamente debe contar con artes de etiqueta de envase y empaque aprobados, según corresponda, para su comercialización y distribución, toda vez que estos hacen parte integral del mismo, por cuanto garantizan su calidad, condiciones de almacenamiento y uso adecuado. - ¿Qué puedo hacer con un ingrediente que no está relacionado en los listados de las entidades de referencias para sustancias permitidas en suplementos dietarios descritas en el anexo 3 del Decreto 3863 de 2008?
- Acorde a lo establecido en el artículo 10 del Decreto 3863 de 2008, cuando los ingredientes, aditivos y sustancias no se encuentren en las referencias citadas en el Anexo 3 del decreto antes mencionado, deberán ser evaluados por la Sala Especializada de Productos Naturales de la Comisión Revisora del Instituto Nacional de Vigilancia de Medicamentos y Alimentos, Invima, o quien haga sus veces, quien elaborará un listado de los nuevos ingredientes aceptados para suplementos dietarios en Colombia, el cual deberá ser actualizado y publicado en la página web del Instituto. Se debe recordar que este trámite es independiente a la solicitud del registro sanitario y tiene un valor independiente, ajustado a la tarifa actual y vigente.
- Para la evaluación de un nuevo ingrediente, aditivo o sustancia, el interesado deberá soportar su solicitud, adjuntando la siguiente información:
- Nombre y dirección del solicitante.
- Nombre del nuevo(s) ingrediente(s) del suplemento dietario. Si es una nueva planta o botánico se debe incluir el nombre científico y Ia parte de Ia planta utilizada.
- Contenido del nuevo ingrediente en el producto.
- Modo de uso del producto.
- Soporte bibliográfico, toxicidad o presentación de los estudios de toxicidad elaborados sobre el producto, si es del caso.
- Referencia a publicaciones de carácter científico y estudios científicos disponibles con sus respectivas copias y traducido al castellano.
- Pago de Ia tarifa por los derechos de evaluación
- El tiempo de evaluación de cada trámite, en la Sala Especializada de Productos Fitoterapéuticos y Suplementos Dietarios dependerá del volumen de trabajo que esta sala posea, así como del orden de radicación de los trámites.
- ¿Dónde puedo encontrar información sobre las condiciones y requisitos que debe cumplir el rotulado o etiquetado de los suplementos dietarios que declaren o no información nutricional, propiedades nutricionales, propiedades de salud a todos para los suplementos dietarios para consumo humano envasados y/o empacados?
- Cuando hayan dudas sobre lo antes mencionado, podemos encontrar respuesta en la Resolución número 3096 de 2007.
- ¿Dónde puedo encontrar información sobre los costos de los diferentes trámites que aplican para suplementos dietarios?
- Los valores de las tarifas vigentes que aplican para los productos suplementos dietarios se pueden encontrar aquí.
Allí encontrará todo lo referente en el manual tarifario vigente para el año 2018. Dicho manual se encuentra en formato Excel. - Si un suplemento dietario tiene asignada una vida útil de 24 meses y dado que no sustenta una vida útil superior a lo establecido en el Decreto 3249 de 2006 (36 meses), ¿es obligatoria la presentación de estudios de estabilidad para el trámite de registro o renovación del registro sanitario?
- De conformidad con lo establecido en el Artículo 11, numeral 2.3 del Decreto 3249 de 2006, mientras no se solicite un tiempo de vida útil superior a 24 meses para un Suplemento Dietario, la norma no obliga a presentar estudios de estabilidad para efectos de la solicitud inicial de Registro Sanitario o de Renovaciones posteriores del mismo. No obstante, cabe aclarar que conforme los lineamientos establecidos en las Buenas Prácticas de Manufactura, los estudios de estabilidad tienen como propósito proveer la evidencia necesaria y suficiente para sustentar el tiempo de vida útil de cualquier producto, permitiendo así establecer la fecha de expiración general para los lotes que se manufacturan bajo las condiciones que establece el fabricante, con lo cual se asegura que, para el caso de un suplemento dietario, el producto mantendrá a través de dicho tiempo, sus características iniciales de calidad, seguridad y aporte nutricional durante toda la etapa de post-mercadeo.
- Además, tales estudios resultan relevantes en cuanto a que permiten predecir el comportamiento general del producto conociendo la variación en el tiempo de sus características físicas, químicas, microbiológicas, de actividad biológica, entre otras, posibilitando así realizar los ajustes que sean requeridos para el desarrollo óptimo y la mejora continua en la estabilidad de la formulación del mismo.
- Por tales motivos y considerando que los suplementos dietarios se caracterizan por ser productos de composición bastante compleja con múltiples ingredientes incluidos dentro de sus formulaciones, siempre se recomienda que se lleven a cabo dichos estudios, iniciándolos de forma previa a la solicitud de registro sanitario, y que se encuentre completa la ejecución de los mismos, una vez ya se estén surtiendo los trámites para la renovación del registro.
- ¿Es de obligatorio cumplimiento lo conceptuado en la Resolución 2015 de 2011, en cuanto lo conceptuado a la realización de estudios de estabilidad?
- Se aclara que la Resolución 2015 de 2011 se encuentra vigente y tiene como finalidad expedir la guía con los lineamientos básicos en Buenas Prácticas de Manufactura – BPM que deben cumplir las fábricas de alimentos que se dediquen a la manufactura, semielaboración o acondicionamiento de suplementos dietarios. Dicha Resolución emana del Artículo 7º del Decreto 3249 de 2006, modificado por el Artículo 2º del Decreto 3863 de 2008. Así mismo, cabe señalar que los lineamientos de estabilidad descritos en el numeral 15.2 de la mencionada Resolución resultan perfectamente equiparables con los ya estipulados en el numeral 15 del Anexo 2 del Decreto 3249 de 2006 complementados por el Anexo 2 del Decreto 3863 de 2008.
Es la etapa en la que se determina si existe responsabilidad por el presunto incumplimiento de la normatividad sanitaria de quienes son sujetos de la inspección, vigilancia y control que ejerce la entidad a productos o establecimientos fraudulentos.
Las Buenas Prácticas de Manufactura (BPM) son todas aquellas medidas adoptadas con el fin de asegurar que los productos farmacéuticos sean de la calidad necesaria para el uso al que están destinados. Todas estas actividades (garantía de calidad, control de calidad, validación, saneamiento e higiene, manejo de quejas, producción, retiro del producto del mercado, auditorias de calidad, personal, equipos, instalaciones, documentación, entre otros) deben asegurar que los productos farmacéuticos estén diseñados y elaborados de tal forma que se tengan en cuenta los requisitos definidos.
Normas BPM Productos Fitoterapéuticos
- Decreto 4927 de 2009 - Por el cual se modifica el Decreto 2266 de 2004 y se dictan otras disposiciones.
- Decreto 1156 de 2018 - Por el cual se reglamenta el régimen de registro sanitario de productos fitoterapéuticos y se dictan otras disposiciones.
- Decreto 3553 de 2004 - Por el cual se modifica el Decreto 2266 de 2004 y se dictan otras disposiciones.
- Resolución 5107 de 2005 - Por la cual se adopta el instrumento de verificación de cumplimiento de condiciones sanitarias para los laboratorios que elaboren productos fitoterapéuticos.
- Resolución 2266 de 2004 - Por el cual se reglamentan los regímenes de registros sanitarios, y de vigilancia y control sanitario y publicidad de los productos fitoterapéuticos.
- Resolución 3131 de 1998 - Por el cual se adopta el Manual de Buenas Prácticas de Manufactura de productos farmacéuticos con base en Recursos Naturales Vigentes.
Normas BPM Suplementos Dietarios
- Resolución 2015 de 2011 - Por la cual se expide la Guía de Inspección de Buenas Prácticas de Manufactura en plantas o fábricas de alimentos que fabriquen, acondicionen o semielaboren suplementos dietarios y se dictan otras disposiciones.
- Decreto 3863 de 2008 - Por el cual se modifica el Decreto 3249 de 2006 y se dictan otras disposiciones.
- Decreto 3249 de 2006 - Por el cual se reglamenta la fabricación, comercialización, envase, rotulado o etiquetado, régimen de registro sanitario, de control de calidad, de vigilancia sanitaria y control sanitario de los suplementos dietarios, se dictan otras disposiciones y se deroga el Decreto 3636 de 2005.
Normas BPM Medicamentos Homeopáticos
- Decreto 1861 de 2006 - Por el cual se modifica y adiciona el Decreto 3554 de 2004 y se dictan otras disposiciones.
- Decreto 3554 de 2004 - Por el cual se regula el régimen de registro sanitario, vigilancia y control sanitario de los medicamentos homeopáticos para uso humano y se dictan otras disposiciones.
- Decreto 4858 de 2007 - Por el cual se modifica el artículo 26 del Decreto 1861 de 2006.
- Resolución 3665 de 2009 - Por la cual se adopta la Guía de Verificación de Cumplimiento de Buenas Prácticas de Manufactura de Medicamentos Homeopáticos y se dictan otras disposiciones.
- Resolución 4594 de 2007 - Por la cual se expide el Manual de Buenas Prácticas de Manufactura para Medicamentos Homeopáticos y se dictan otras disposiciones.
Año 2025
- Diciembre 2025
- Noviembre 2025
- Octubre 2025
- Septiembre 2025
- Agosto 2025
- Julio 2025
- Junio 2025
- Mayo 2025
- Abril 2025
- Marzo 2025
- Febrero 2025
- Enero 2025
Año 2024
- Diciembre 2024
- Noviembre 2024
- Octubre 2024
- Septiembre 2024
- Agosto 2024
- Julio 2024
- Junio 2024
- Mayo 2024
- Abril 2024
- Marzo 2024
- Febrero 2024
- Enero 2024
Año 2023
- Diciembre 2023
- Noviembre 2023
- Octubre 2023
- Septiembre 2023
- Agosto 2023
- Julio 2023
- Junio 2023
- Mayo 2023
- Abril 2023
- Marzo 2023
- Febrero 2023
- Enero 2023
Año 2022
- Diciembre 2022
- Noviembre 2022
- Octubre 2022
- Septiembre 2022
- Julio 2022
- Junio 2022
- Mayo 2022
- Abril 2022
- Marzo 2022
- Febrero 2022
- Enero 2022
Año 2021
- Diciembre 2021
- Noviembre 2021
- Octubre 2021
- Septiembre 2021
- Agosto 2021
- Julio 2021
- Junio 2021
- Mayo 2021
- Abril 2021
- Marzo 2021
- Febrero 2021
- Enero 2021
Año 2020
- Diciembre 2020
- Noviembre 2020
- Octubre 2020
- Septiembre 2020
- Agosto 2020
- Julio 2020
- Junio 2020
- Mayo 2020
- Abril 2020
- Marzo 2020
- Febrero 2020
- Enero 2020
Año 2019
- Noviembre 2019
- Octubre 2019
- Septiembre 2019
- Agosto 2019
- Julio 2019
- Junio 2019
- Mayo 2019
- Abril 2019
- Marzo 2019
- Febrero 2019
- Enero 2019
Año 2018
- Enero 2018
- Febrero 2018
- Marzo 2018
- Abril 2018
- Mayo 2018
- Junio 2018
- Julio 2018
- Agosto 2018
- Septiembre 2018
- Octubre 2018
- Noviembre 2018
- Diciembre 2018
Año 2017
- Diciembre 2017
- Noviembre 2017
- Octubre 2017
- Septiembre 2017
- Agosto 2017
- Junio 2017
- Mayo 2017
- Abril 2017
- Marzo 2017
- Febrero 2017
- Enero 2017
Año 2016
Año 2025
- Diciembre 2025
- Noviembre 2025
- Octubre 2025
- Septiembre 2025
- Agosto 2025
- Julio 2025
- Junio 2025
- Mayo 2025
- Abril 2025
- Marzo 2025
- Febrero 2025
- Enero 2025
Año 2024
- Diciembre 2024
- Noviembre 2024
- Octubre 2024
- Septiembre 2024
- Agosto 2024
- Julio 2024
- Junio 2024
- Mayo 2024
- Abril 2024
- Marzo 2024
- Febrero 2024
- Enero 2024
Año 2023
- Diciembre 2023
- Noviembre 2023
- Octubre 2023
- Septiembre 2023
- Agosto 2023
- Julio 2023
- Junio 2023
- Mayo 2023
- Abril 2023
- Marzo 2023
- Febrero 2023
- Enero 2023
Año 2022
- Diciembre 2022
- Noviembre 2022
- Octubre 2022
- Septiembre 2022
- Julio 2022
- Junio 2022
- Mayo 2022
- Abril 2022
- Marzo 2022
- Febrero 2022
- Enero 2022
Año 2021
- Diciembre 2021
- Noviembre 2021
- Octubre 2021
- Septiembre 2021
- Agosto 2021
- Julio 2021
- Junio 2021
- Mayo 2021
- Abril 2021
- Marzo 2021
- Febrero 2021
- Enero 2021
Año 2020
- Diciembre 2020
- Noviembre 2020
- Octubre 2020
- Septiembre 2020
- Agosto 2020
- Julio 2020
- Junio 2020
- Mayo 2020
- Abril 2020
- Marzo 2020
- Febrero 2020
- Enero 2020
Año 2019
- Noviembre 2019
- Octubre 2019
- Septiembre 2019
- Agosto 2019
- Julio 2019
- Junio 2019
- Mayo 2019
- Abril 2019
- Marzo 2019
- Febrero 2019
- Enero 2019
Año 2018
- Enero 2018
- Febrero 2018
- Marzo 2018
- Abril 2018
- Mayo 2018
- Junio 2018
- Agosto 2018
- Septiembre 2018
- Octubre 2018
- Noviembre 2018
- Diciembre 2018
Año 2017
- Diciembre 2017
- Noviembre 2017
- Octubre 2017
- Septiembre 2017
- Agosto 2017
- Junio 2017
- Mayo 2017
- Abril 2017
- Marzo 2017
- Febrero 2017
- Enero 2017
Año 2016
Año 2025
- Diciembre 2025
- Noviembre 2025
- Octubre 2025
- Septiembre 2025
- Agosto 2025
- Julio 2025
- Junio 2025
- Mayo 2025
- Abril 2025
- Marzo 2025
- Febrero 2025
- Enero 2025
Año 2024
- Diciembre 2024
- Noviembre 2024
- Octubre 2024
- Septiembre 2024
- Agosto 2024
- Julio 2024
- Junio 2024
- Mayo 2024
- Abril 2024
- Marzo 2024
- Febrero 2024
- Enero 2024
Año 2023
- Diciembre 2023
- Noviembre 2023
- Octubre 2023
- Septiembre 2023
- Agosto 2023
- Julio 2023
- Junio 2023
- Mayo 2023
- Abril 2023
- Marzo 2023
- Febrero 2023
- Enero 2023
Año 2022
- Diciembre 2022
- Noviembre 2022
- Octubre 2022
- Septiembre 2022
- Julio 2022
- Junio 2022
- Mayo 2022
- Abril 2022
- Marzo 2022
- Febrero 2022
- Enero 2022
Año 2021
- Diciembre 2021
- Noviembre 2021
- Octubre 2021
- Septiembre 2021
- Agosto 2021
- Julio 2021
- Junio 2021
- Mayo 2021
- Abril 2021
- Marzo 2021
- Febrero 2021
- Enero 2021
Año 2020
- Diciembre 2020
- Noviembre 2020
- Octubre 2020
- Septiembre 2020
- Agosto 2020
- Julio 2020
- Junio 2020
- Mayo 2020
- Abril 2020
- Marzo 2020
- Febrero 2020
- Enero 2020
Año 2019
- Noviembre 2019
- Octubre 2019
- Septiembre 2019
- Agosto 2019
- Julio 2019
- Junio 2019
- Mayo 2019
- Abril 2019
- Marzo 2019
- Febrero 2019
- Enero 2019
Año 2018
- Enero 2018
- Febrero 2018
- Marzo 2018
- Abril 2018
- Mayo 2018
- Junio 2018
- Julio 2018
- Agosto 2018
- Septiembre 2018
- Octubre 2018
- Noviembre 2018
- Diciembre 2018
Año 2017
- Diciembre 2017
- Noviembre 2017
- Octubre 2017
- Septiembre 2017
- Agosto 2017
- Junio 2017
- Mayo 2017
- Abril 2017
- Marzo 2017
- Febrero 2017
- Enero 2017
Año 2016
Año 2025
- Diciembre 2025
- Noviembre 2025
- Octubre 2025
- Septiembre 2025
- Agosto 2025
- Julio 2025
- Junio 2025
- Mayo 2025
- Abril 2025
- Marzo 2025
- Febrero 2025
- Enero 2025
Año 2024
- Diciembre 2024
- Noviembre 2024
- Octubre 2024
- Septiembre 2024
- Agosto 2024
- Julio 2024
- Junio 2024
- Mayo 2024
- Abril 2024
- Marzo 2024
- Febrero 2024
- Enero 2024
Año 2023
- Diciembre 2023
- Noviembre 2023
- Octubre 2023
- Septiembre 2023
- Agosto 2023
- Julio 2023
- Junio 2023
- Mayo 2023
- Abril 2023
- Marzo 2023
- Febrero 2023
- Enero 2023
Año 2022
- Diciembre 2022
- Noviembre 2022
- Octubre 2022
- Septiembre 2022
- Julio 2022
- Junio 2022
- Mayo 2022
- Abril 2022
- Marzo 2022
- Febrero 2022
- Enero 2022
Año 2021
- Diciembre 2021
- Noviembre 2021
- Octubre 2021
- Septiembre 2021
- Agosto 2021
- Julio 2021
- Junio 2021
- Mayo 2021
- Abril 2021
- Marzo 2021
- Febrero 2021
- Enero 2021
Año 2020
- Diciembre 2020
- Noviembre 2020
- Octubre 2020
- Septiembre 2020
- Agosto 2020
- Julio 2020
- Junio 2020
- Mayo 2020
- Abril 2020
- Marzo 2020
- Febrero 2020
- Enero 2020
Año 2019
- Noviembre 2019
- Octubre 2019
- Septiembre 2019
- Agosto 2019
- Julio 2019
- Junio 2019
- Mayo 2019
- Abril 2019
- Marzo 2019
- Febrero 2019
- Enero 2019
Año 2018
- Enero 2018
- Febrero 2018
- Marzo 2018
- Abril 2018
- Mayo 2018
- Junio 2018
- Julio 2018
- Agosto 2018
- Septiembre 2018
- Octubre 2018
- Noviembre 2018
- Diciembre 2018
Año 2017
- Diciembre 2017
- Noviembre 2017
- Octubre 2017
- Septiembre 2017
- Agosto 2017
- Julio 2017
- Junio 2017
- Mayo 2017
- Abril 2017
- Marzo 2017
- Febrero 2017
- Enero 2017
Año 2016
¿A qué establecimientos les aplican las Buenas Prácticas de Manufactura (BPM)?
Aplica a los laboratorios o establecimientos farmacéuticos que fabriquen, procesen, envasen y/o acondicionen productos farmacéuticos o aquellos que deseen ampliar el concepto técnico respecto a productos, áreas de manufactura, actividades y procesos productivos, ubicados en el territorio nacional y en el exterior.
¿Qué grupo atiende las inquietudes con respecto a Buenas Prácticas de Manufactura (BPM) de Productos Fitoterapéuticos, Suplementos Dietarios o Medicamentos Homeopáticos?
El grupo que atiende este tipo de inquietudes es el Grupo Técnico de Medicamentos y Productos Biológicos del Invima, conformado por un equipo multidisciplinario, que previo estudio de las inquietudes planteadas por los usuarios da respuesta a las mismas lo más pronto posible, conforme a los tiempos estipulados.
Los canales disponibles para comunicarse con el grupo son: vía telefónica (Teléfono: 2948700, Extensión: 3921 y 3847) o a través de cita programada con la Dirección de Medicamentos y Productos Biológicos a través del siguiente link: Canales de Atención al Ciudadano.
¿En dónde puedo encontrar el manual tarifario vigente?
Las tarifas para los servicios que presta el Invima se encuentran en la página www.inima.gov.co en el recuadro de “Trámites y Servicios” en “Tarifas Vigentes”.
¿Cuál es la tarifa correspondiente a la emisión de un certificado de Buenas Prácticas de Manufactura (BPM) de productos fitoterapéuticos, suplementos dietarios o medicamentos homeopáticos?
Las tarifas para los servicios que presta el Invima están definidas mediante Resolución. La emisión del certificado de BPM o cualquier otro documento relacionado, puede ser consultada en el manual tarifario que se puede consultar en la página www.invima.gov.co en el recuadro de “Trámites y Servicios” en “Tarifas Vigentes”. La emisión de certificados de BPM, se encuentran dentro de la tarifa con código 4008.
¿Cómo puede solicitar un laboratorio o establecimiento autorizado una certificación en Buenas Prácticas de Manufactura (BPM) de productos fitoterapéuticos, suplementos dietarios o medicamentos homeopáticos?
Radicando en la Oficina de Atención al Ciudadano en la sede principal del Invima: Carrera 10 N° 64 – 28 ubicada en Bogotá, los siguientes documentos:
- Recibo de consignación por concepto del trámite solicitado (Copia emitida por la entidad bancaria).
Certificado de existencia y representación legal del establecimiento. - Guía de inspección dada mediante Resolución 5107 de 2005 para Fitoterapéuticos, Resolución 2015 de 2011 para suplementos dietarios y Resolución 3665 de 2009 para homeopáticos debidamente diligenciada.
- Copia de la tarjeta profesional del Director Técnico y el vínculo laborar suscrito con la empresa.
- Poder debidamente legalizado (en caso de que se actué por medio apoderado) y diligenciado el formato solicitud de trámites (visitas, certificados y certificados), ASS-AYC-FM033, disponible para su descargue en página web del Instituto: www.invima.gov.co, a través de la siguiente ruta: Trámites y Servicios -Trámites - Seleccione Grupo (Medicamentos síntesis química y biológicos) - Seleccione Trámite... (Visitas, certificaciones y certificados de BPM) – Formatos - Formato de Solicitud de Trámites (Visitas, Certificación y Certificados).
¿Los establecimientos dedicados al acondicionamiento de productos farmacéuticos requieren certificación en BPM?
Sí, el acondicionamiento de productos farmacéuticos (etiquetado, codificado, desestuchado y/o empaque) es considerado como una etapa productiva más dentro de todo el proceso de fabricación.
¿Un establecimiento dedicado únicamente al almacenamiento de productos farmacéuticos requiere la certificación de BPM para funcionar?
No, hasta el momento la certificación en BPM no es un requisito para que este tipo de establecimientos funcione desde las competencias del Instituto.
¿Qué tipo de cambios que realice un establecimiento farmacéutico en cuanto a la certificación en Buenas Prácticas de Manufactura (BPM) de Productos fitoterapéuticos, suplementos Dietarios o medicamentos homeopáticos, deben ser informados al Invima?
Cualquier modificación que se haga en las condiciones evaluadas y certificadas, respecto a equipos, áreas, procesos productivos, personal técnico principal o de las empresas con las que se contrató la realización de actividades críticas de producción y control de calidad, deberán ser notificadas al Invima con el fin de que éste evalúe y verifique si se requiere una visita de ampliación o verificación del concepto técnico emitido, de acuerdo con las disposiciones de la Normatividad Sanitaria correspondiente.
Los documentos a presentarse por parte del responsable sanitario o director técnico deben prepararse de acuerdo a la guía publicada en la página web del Instituto: www.invima.gov.co, a través de la siguiente ruta: Aseguramiento Sanitario - Inspección, vigilancia control – FORMATOS - Guías y Formatos de la Dirección de Medicamentos y Productos Biológicos - Guía para la notificación de cambio de las condiciones certificadas por la Dirección de Medicamentos y Productos Biológicos.
¿Qué condiciones deben cumplir los certificados de BPM provenientes de otros países?
Estos certificados deben cumplir con lo descrito en la normatividad sanitaria vigente: Decreto 459 DE 2001 “Por el cual se establece el procedimiento para la obtención del Certificado de Cumplimiento de la Buenas Prácticas de Manufactura por parte de los laboratorios fabricantes de medicamentos que se importen o produzcan en el país” y el Decreto 162 DE 2004 “Por el cual se modifica el artículo 3° del Decreto 549 de 2001”.
¿Cómo puede consultarse el estado de conformidad y vigencia de una certificación en BPM de laboratorios o establecimientos farmacéuticos?
La consulta puede realizarse en la página web del Instituto: www.invima.gov.co, a través de la siguiente ruta: Aseguramiento Sanitario - Inspección, vigilancia control – Establecimientos vigilados - Establecimientos autorizados de Medicamentos y Productos Biológicos.
¿Cómo se solicita una visita de certificación, renovación o ampliación en BPM de productos fitoterapéuticos, suplementos dietarios o medicamentos homeopáticos?
Una vez el interesado considere que ha dado cumplimiento a los requisitos técnicos y legales establecidos en la normatividad sanitaria, debe presentar ante el Invima la solicitud de visita, anexando para ello los documentos que indica la página web del Instituto: www.invima.gov.co, a través de la siguiente ruta: Trámites y Servicios – Trámites – Seleccione Grupo… (Medicamentos síntesis química y biológicos) – Seleccione Trámite... (Escoja la que se ajuste a su búsqueda entre: visitas, certificaciones y certificados de BPM), en donde se relacionan los requisitos, información asociada, formatos y tarifas. Esta documentación debe ser radicada en la Oficina de Atención al Ciudadano en la sede principal del Invima: carrera 10 N° 64 – 28 ubicada en Bogotá.
¿Cuánto tiempo demora la programación de la visita de certificación, renovación o ampliación en BPM de productos fitoterapéuticos, suplementos dietarios o medicamentos homeopáticos?
La definición de la fecha de realización de la visita depende de la programación generada por el Grupo Técnico de Medicamentos y Productos Biológicos del Invima, teniendo en cuenta las solicitudes incluidas en la base de datos, la fecha de radicación y los términos establecidos por la normatividad vigente.
¿Qué sucede cuando se cancela la certificación en BPM de productos fitoterapéuticos, suplementos dietarios o medicamentos homeopáticos?
Los laboratorios o establecimientos farmacéuticos que pierden la certificación en Buenas Prácticas de Manufactura (BPM) de productos fitoterapéuticos, suplementos dietarios o medicamentos homeopáticos, están imposibilitados para realizar procesos y actividades productivas de fabricación, procesos de envase, acondicionamiento, distribución, comercialización y análisis de control de calidad de productos farmacéuticos, ubicados en el territorio nacional y en el exterior. Para el caso de las certificaciones de fuera del país, se les niega o suspende su importación. En este caso deben solicitar de nuevo la visita de certificación conforme a lo normativamente vigente y establecido en materia sanitaria.
¿Qué requisitos deben cumplir los laboratorios o establecimientos farmacéuticos que quieran certificarse en BPM de suplementos dietarios?
Los requisitos aparecen estipulados en el artículo 2 del Decreto 3863 de 2008.
Para los laboratorios o establecimientos que no se dedican exclusivamente a la fabricación de suplementos dietarios, que se fabriquen en plantas donde se elaboren medicamentos o productos fitoterapeúticos, deben tramitar ante el Invima, una autorización de fabricación de estos productos en dichas plantas, para lo cual deberá adjuntar los respectivos soportes de validación de limpieza.
Dicha autorización debe tramitarse de manera independiente a la obtención del certificado de Buenas Prácticas de Manufactura (BPM). En casos especiales, o si el Invima lo considera pertinente, podrá verificar en la planta el cumplimiento de los procesos de validación de limpieza presentados.
La autorización para la fabricación de los suplementos dietarios en laboratorios que fabriquen medicamentos o productos fitoterapeúticos estará sujeta al mantenimiento de las condiciones bajo las cuales se otorgaron las Buenas Prácticas de Manufactura (BPM).
¿Los establecimientos que elaboran medicamentos homeopáticos magistrales u oficinales no estériles, deben contar con BPM para realizar esta actividad?
No. Conforme lo establece el Decreto 1737 de 2005: “Por el cual se reglamenta la preparación, distribución, dispensación, comercialización, etiquetado, rotulado y empaque de los medicamentos homeopáticos magistrales y oficinales y se dictan otras disposiciones”, las farmacias homeopáticas autorizadas que efectúan las operaciones de carácter técnico, que comprenden la elaboración de la fórmula magistral o medicamento oficinal, bajo una forma farmacéutica determinada, así como su control y acondicionamiento, deben seguir las Buenas Prácticas de Preparación (BPP), de medicamentos homeopáticos magistrales y oficinales conforme a la reglamentación que para tal efecto expida el Ministerio de la Protección Social.
¿Cuál es el tiempo de vigencia de una certificación en BPM de productos fitoterapéuticos, suplementos dietarios o medicamentos homeopáticos?
La vigencia de una certificación de cumplimiento de Buenas Prácticas de Manufactura (BPM) de productos fitoterapéuticos, suplementos dietarios y medicamentos homeopáticos es de cinco (5) años, todos los términos contados a partir de la fecha ejecutoria del acto que la concede.
¿Busca información más reciente o detallada?
Consulte nuestro nuevo buscador dinámico de Certificaciones y Listados Oficiales
Ver Listados Oficiales (BPM Homeopáticos, Fitoterapéuticos y Suplementos Dietarios).


